
▲高端宣布解盲成功,總經理陳燦堅對取得國內EUA很樂觀,正準備申請歐盟等國外認證。
圖文/鏡週刊
本刊調查,二家國產疫苗除將申請緊急使用授權(EUA)在國內開打,也三路並進、布局海外市場以取得國際認證。不過,以時程估算,二家國產疫苗最快今年底才有可能取得國際認證,屆時施打國產疫苗的民眾,仍可能面臨半年空窗期,即入境他國的檢疫方式異於施打其他國際大廠疫苗者。
以高端為例,成功解盲後,除向食藥署申請EUA,另也宣布向歐盟申請臨床試驗,但就時程估算,最快也要到年底才能完成試驗、取得認證。
對此,高端高層接受本刊採訪說,國產疫苗屬蛋白疫苗,較穩定、無嚴重副作用,現階段任務是「先讓台灣人保命」,有商務出國需求者,建議政府讓人民評估可承受的副作用後,自行選擇疫苗廠牌解決。
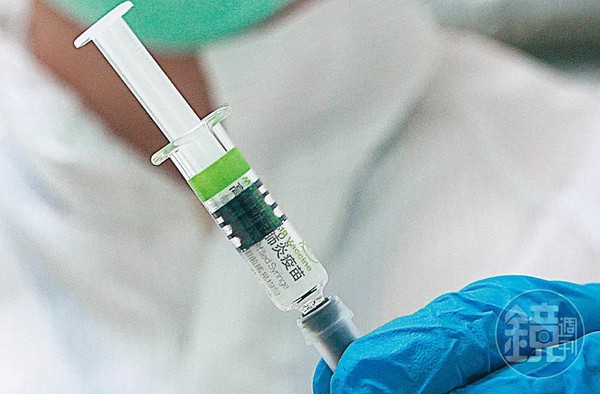
▼高端疫苗生產的「預充填針劑」已有26.7萬支交由食藥署「檢驗封緘」,一旦通過EUA即可快速出貨。
衛福部長陳時中在立法院備詢時也坦言,國產疫苗的確有無法及時得到國際認證的風險,後續等預約系統上路、國外疫苗陸續到位,就可開放選擇。

更多鏡週刊報導
【國產疫苗攻海外4】國產疫苗保護力掀戰火 專家要政府做一件事
【獨家】【國產疫苗攻海外】菲律賓來函「台灣EUA審過就認」 國產疫苗可望銷往東南亞
【獨家】【國產疫苗攻海外1】友邦獨家文件曝光 高端將前進中南美臨床









讀者迴響