
▲南韓總統文在寅表示,將全方位支援SK生技進行國產疫苗第3期臨床實驗。圖為文在寅2020年10月前往SK生技位於京畿道城南市的細胞培養室。(圖/達志影像)
記者羅翊宬/編譯
隨著新冠病毒持續變種,各國積極展開國產疫苗的研發進程,南韓政府更於10日正式通過SK Bioscience國產疫苗「GBP510」的第3期臨床實驗,將採免疫橋接方式,與阿斯特捷利康(AZ)疫苗進行抗體濃度比對,最快可望明年初上市。不過SK的國產疫苗在未來還得面臨層層考驗,包括能否通過國際認證、在銷售市場上與mRNA疫苗的競爭、能否對抗變種病毒。
根據韓媒《週間東亞》,SK公司的國產疫苗GBP510採用重組蛋白疫苗技術,第3期臨床實驗將採免疫橋接進行,是繼法國藥廠Valneva的國產疫苗VLA2001後,全球第2支採用免疫橋接進行臨床實驗的疫苗,在參與臨床實驗的3990人中,有3000人施打受試疫苗、另外990人施打AZ疫苗。
即便SK的國產疫苗成功於明年上市,恐怕還得面臨層層難關!因為隨著AZ疫苗出現血栓疑慮,導致包括南韓、澳洲、歐洲等暫緩AZ與嬌生疫苗施打,全球各國反更加偏好輝瑞(BNT)、莫德納等mRNA疫苗,而SK的GBP510則是重組蛋白疫苗,未來是否能喚起各國政府興趣、增加需求量仍是未知數。
且由於SK的GBP510是專門為新冠肺炎爆發初期的病毒量身打造,究竟是否能有效對抗Delta等變種病毒,仍須同時進行研究。
▼南韓SK生技研發的國產疫苗GBP510。(圖/達志影像)
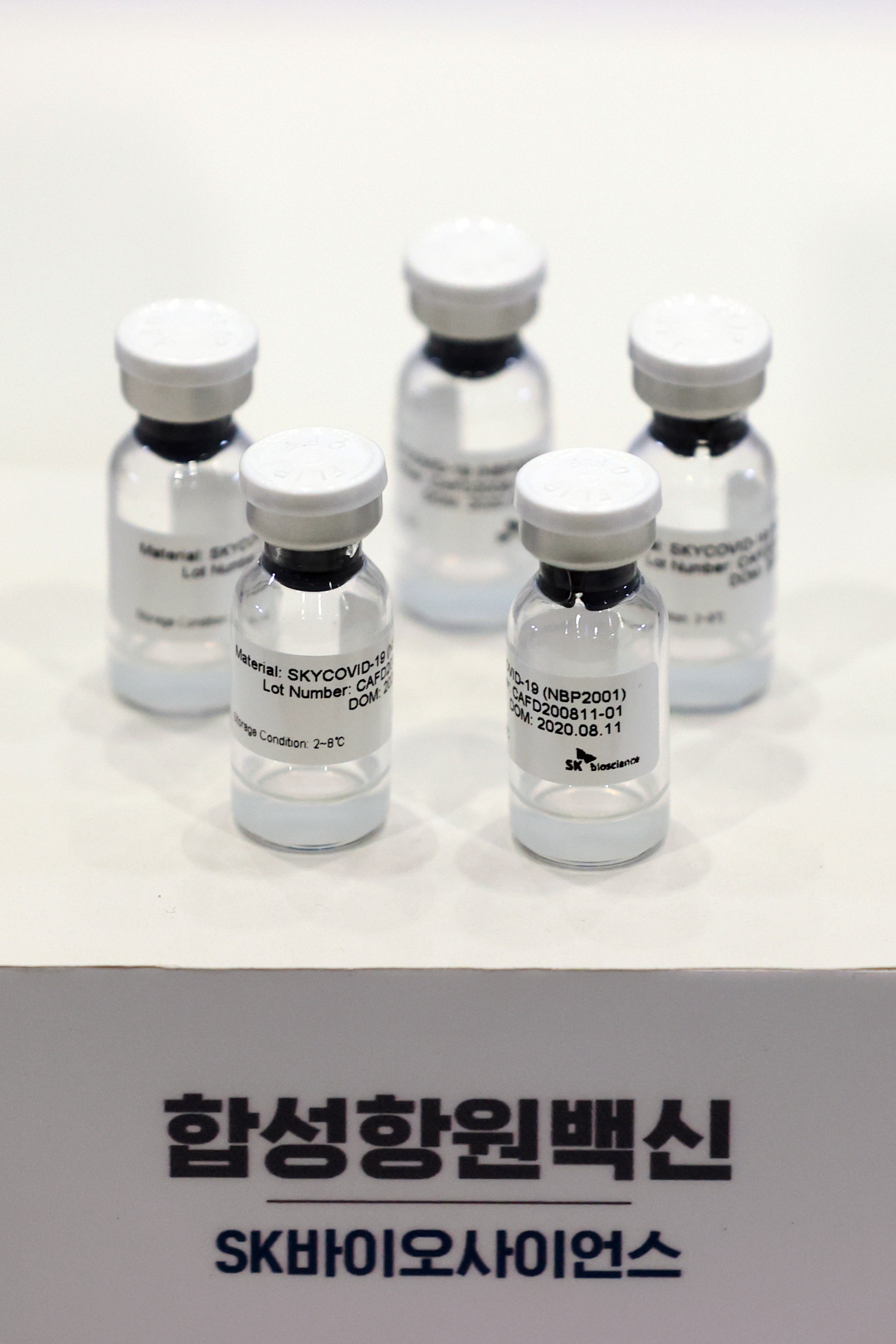
不過,SK的GBP510也並非完全喪失優勢!翰林大學江南聖心醫院感染內科教授李載甲(이재갑,音譯)認為,目前亞洲與非洲至今為止的接種覆蓋率仍未超過1%,因此在全球大流行之際,國產疫苗不可能無法成功對外出口。
國際疫苗研究所(IVI)所長傑羅姆金(Jerome Kim)則表示,SK與諾瓦瓦克斯研發的重組蛋白疫苗在價格上具有競爭力,且疫苗的冷藏溫度適用於大部分國家,可望成為mRNA疫苗的替代方案,為全球尚未接種第2劑疫苗的75%人口增添助益,此外也可當成第3劑「加強針」來施打。SK表示,GBP510的保存期限較長,且可保存在常溫攝氏2至8度的環境。











讀者迴響