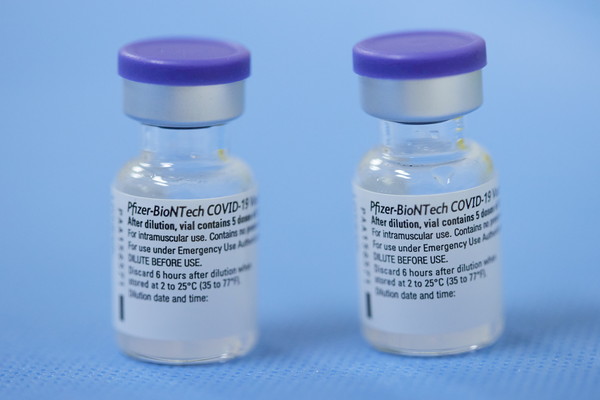
▲德國BioNTech新冠疫苗、BNT疫苗。(圖/路透社)
記者李佳蓉/綜合報導
輝瑞/BNT於美國時間20日發出聲明,表示BNT疫苗對5~11歲族群安全且可產生極佳中和抗體,預計將於本月底向美國食品藥品監督管理局(FDA)申請該族群之緊急使用授權(EUA)。若屆時通過後,台灣是否跟進,讓幼童即早接種疫苗?前台大感染科醫師林氏璧從2面向評估「完全不急」。
家醫科醫師陳欣湄觀察,新冠病毒對於幼童的重症率低於成人,但隨著Delta變種病毒出現,5至12歲的孩子感染機率也跟著上升,出現感染幼童化的趨勢。
前台大感染科醫師林氏璧在粉專《日本自助旅遊中毒者》發文,指出輝瑞/BNT發布臨床試驗結果,在5~11歲兒童收案2268人,劑量為是10ug,是12歲以上1/3,接種2劑疫苗,施打間隔為21天。該試驗在美國、芬蘭、波蘭、西班牙等超過90個醫學中心執行,結果發現在第二劑後28天所測得的中和抗體,與先前16~25歲接種30ug疫苗後反應相當,輝瑞/BNT預計將此第三期臨床試驗投稿,並送交法規單位進行緊急授權使用。

▲BNT若通過5~11歲EUA,台灣是否跟進,前台大醫認為「還不急」。(示意圖/取自免費圖庫Pexels)
林氏璧解讀,新聞稿中僅有提到2組不良反應相當,還沒有公布詳情,「當然2千人的資料是看不太到心肌炎的」,預估這下FDA又有得忙了,因為11歲以下施打mRNA疫苗完全是新的領域,審查委員肯定相當關心大量施打下是否產生不良反應。
林氏璧接著說,最後2個年齡段也還在進行臨床試驗,包括2~5歲及6個月~2歲的資料,預計今年第4季會有結果。至於台灣要不要跟進,他認為「完全不急」,可先觀察接下來美國若大量施打兒童後的不良反應通報,還有真實世界的有效數字出來,謹慎評估風險和獲益再決定即可。









讀者迴響